КОНТРОЛЬ БАКТЕРИЙНЫХ ПРЕПАРАТОВ
Спасибо нашим инвесторам из казино онлайн
КОНТРОЛЬ БАКТЕРИЙНЫХ ПРЕПАРАТОВ
(вакцин) как гос. контроль вакцин и леч. сывороток введен в РСФСР в 1919 г. и сосредоточен в Москве в Ин-те экспериментальной терапии и контроля сывороток и вакцин им. Тарасевича. Все вакцины, леч. сыворотки и другие бактерийные препараты (оспенный детрит, анатоксины, тестику-лярная жидкость и т. п.), применяемые на людях в качестве леч. или предохранительных средств, предварительно контролируются в этом ин-те. Признанный годным препарат получает контрольный номер и только тогда допускается к обращению и употреблению. Контрольный институт обслуживает также нек-рые другие республики СССР (Белоруссию, отчасти Украину, Азербайджан и др.). Мысль о необходимости единого гос. контроля бактерийных препаратов (по. примеру Германии) высказывалась Л. А. Тарасовичем еще до империалистской войны. Во время войны введение обязательных предохранительных прививок в армии поставило на очередь вопрос о контроле; были организованы три т. н. контрольные станции Земского союза в Москве, Киеве и Смоленске, осуществлявшие частично этот контроль. С упразднением Земского союза в 1918 г. эти функции временно перешли к контрольной станции при Микробиол. ин-те Об-ва московских научных ин-тов. В 1919 г. по инициативе Л. А. Тарасевича и под его управлением она была преобразована в Ин-т контроля сывороток и вакцин НКЗдр. Как показывают прилагаемые кривые (рис. 1—3), количество препаратов, проходящих через ин-т, постепенно растет. Падение количества препаратов в 1923—24 гг. объясняется тем, что с 1923 г. наступило снижение кишечных заболеваний; в дальнейшем производственные функции ин-тов возросли по всем видам бактерийных препаратов. В РСФСР в общих чертах принята нем. система контроля сыво –
«97
роток и вакцин. Во Франции бактерийные препараты почти все без исключения производятся в Пастеровском ин-те; в нем же со –
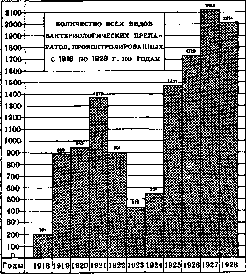
Рисунок 1.
АН»
\,Э! в
7««/
узе
7в4/Г
и& /
иЛ-».
п
Годы
•1921
Рисунок 2. Количество серий вакцин, проконтролированных с 1918 по 1928 г. по годам.
SB2
ЪН/Г
750-700-65Q-600-
Количество серий сывороток прок0нтролир0ванныx
С 1918 по 1928 г. по годам
т/
52»/
л-
^~
L*»
/
не
/
п./ Годы Рисунок 3. средоточен и контроль этих препаратов. В Германии, где бактерийные препараты изготовляются гл. обр. в частных предприятиях, гос. контроль имеет особенно жесткий характер. Все бутыли с готовыми бактерий – ными препаратами опечатываются гос. чиновниками-контролерами и остаются в таком виде впредь до получения контрольного номера из Гос. ин-та экспериментальной терапии во Франкфурте-на-Майне; лишь после этого они допускаются в обращение. Контроль вакцин в СССР состоит в проверке стерильности путем посева вакцины на питательные среды, испытании чистоты взятых штаммов (микроскоп, просмотр мазков) и определении количества микробных тел в 1
см3
вакцины; иногда производится также определение антигенных свойств ее. Методы определения количества микробных тел в эмульсии: 1) непосредственный счет бактерийных тел, 2) счет живых зародышей, 3) определение степени мутности эмульсии, 4) взвешивание бактериальной массы и 5) определение объема осадка при центрифугировании.— Непосредственный счет бактерийных тел всего чаще производится путем счета в счетной камере Тома-Цейса или в какой-либо другой. Счет производится с наибольшей сухой системой, иногда после предварительной окраски микробов, вычис – , &250 000 ление—по формуле:
х = п. т
—-—■, где ж— число бактерий в 1
см3, п
—число сосчитанных бактерий,
т
—число кратности разведений и
q
—число сосчитанных больших квадратов. Счет можно производить также по методу Райта (Wright): в пипетку с длинным оттянутым капиляром насасывают последовательно до метки (отделяя пузырьком воздуха) кровь, lV2%-Hbift раствор лимоннокислого натра и эмульсию бактерий. Все смешивают в луночке предметного стекла; из капельки смеси делают мазок, фиксируют, красят по Мансону (Manson), сосчитывают в нескольких полях зрения количество эритроцитов и количество бактерий и произво – ,& о. 5 000 000 000 дят вычисление по формуле ж =-^—— где
х
= число бактерий в 1
см3, о
—число сосчитанных бактерий и
к
—число сосчитанных эритроцитов. Существует ряд видоизменений первоначального метода Райта. Менее употребительны метод счета окрашенных микробов на покровном стекле (метод Klein’а, Маслаковца), счет смеси пивных дрожжей и бактерий и ряд других. Все вышеперечисленные методы определяют микробы в концентрации от 100.000 до 1.000.000 в 1
см3;
получаемые цифры не вполне точны, с большим или меньшим приближением. Определение бактерий в эмульсии методом посева в агаровую пластинку и счета живых зародышей применяется при приготовлении вакцины, до убивания микробов. Из основной эмульсии делается ряд разведений; 1
см3
каждого разведения смешивается с расплавленным и охлажденным агаром, смесь выливается в чашку Петри, которая ставится. вверх дном на сутки или двое в термостат при 37°. Число выросших колоний (соответствующее числу живых микробов) определяется при помощи лупы, для чего существуют различные счетные камеры с лупами.—О пределение количества бактерий путем сравнения степени мутности бактериальной эмульсии с
70»
определенным стандартом (степень мутности определяется на просвечиваемость) применяется всего чаще благодаря простоте и быстроте метода, хотя он и обладает лишь приблизительной точностью. Стандартом может служить как бактериальная эмульсия, просчитанная по одному из вышеизложенных методов, так и другие вещества, напр. взвеси нерастворимых солей (сернокислый барий), эмульсия лецитина и др. Имеются специальные приборы, как напр. нефелометр Клейнмана, турбидоколориметр Доль-да (Do Id) и др.—О преде’лени-е количества бактерий путем взвешивания бактерийной массы—метод неточный, т. к. результаты варьируют в зависимости от влажности массы. Возможно также определение количества бактерий в эмульсии по объему осадка, получаемого при центрифугировании; последнее производится в особых центрифужках с оттянутым ка-пиляром, на к-ром нанесены деления.—Для определения антигенных свойств вакцина вводится повторно (2—4 раза под кожу или в вену) нескольким кроликам; через 10— 20 дней у животных берется кровь и в ней определяется количество аглютининов и веществ, связывающих комплемент. Кон т р оль сывороток. Лечебные сыворотки должны удовлетвор
ять следующим требованиям: сыворотка должна быть прозрачна и свободна от грубых осадков; должна быть стерильна, т. е. не содержать никаких живых микроорганизмов; безвредна для животных; в качестве консервирующих веществ может применяться только фенол в количестве не более 0,5%, хлороформ (1%) или трикрезол (0,4%); содержание белка в сыворотке не должно превышать 12%; сыворотка должна соответствовать установленному стандарту.—Полученная на контроль сыворотка подвергается осмотру макроскопически для определения ее прозрачности и присутствия осадков. Затем делается посев на обыкновенный бульон, косой агар и сахарный прямой агар для проверки стерильности. Для испытания безвредности сыворотка вводится под кожу морской свинке в дозе 8—10
см3
и мыши (0,5
см3).
Отсутствие заболевания этих животных исключает присутствие в сыворотке анаэробных микробов (Вас. tetani, возбудителей газовой гангрены) и их токсинов, а также избытка фенола (избыток фенола вызывает отравление мыши, выражающееся дрожью тела). Если к 6-му дню животные остаются совершенно здоровыми, сыворотка годна к употреблению (если конечно она удовлетворяет другим требованиям). В нек-рых случаях (концентрированные сыворотки) сыворотка проверяется на количество содержащегося в ней белка, к-рое не должно превышать 12%, т. к. при высоком содержании белка усиливаются сывороточные явления.—Кроме испытания на стерильность и безвредность сыворотки стандартизуются, т. е. проверяются на специфическую их силу. По способу получения леч. сывороток и по характеру их действия различают 2 типа сывороток: антитоксические и антибактериальные (бактерицидные). Испытания силы сыворотки антитоксической и антибактериальной существенно отличаются друг от друга» Основой определения силы антитоксической сыворотки (стандартизация) является нейтрализация токсина антитоксином. В основу определения силы антибактериальных сывороток положено определение количества бактериальных антител (бактериолизинов,. аглютининов, комплемент связывающих тел и т. п.). В общем можно сказать, что методика определения силы антибактериальных сывороток значительно менее точна, чем методика стандартизации антитоксических сывороток. К антитоксическим сывороткам относятся противодифтерийная, противостолбнячная, противодизентерийная, отчасти противоскарлатинозная и противоган-гренозная. Две последние впрочем часто являются смешанными, т. е. одновременно антитоксическими и антибактериальными. Стандартизация противодифтерийной сыворотки производится в Европе и в Америке по способу Эрлиха на морских свинках. Для производства контроля необходимы стандартная сыворотка, контрольный токсин с точно установленной по стандартной сыворотке: дозой, физиол. раствор NaCl для разведений, серия градуированных на сотые доли
см3
пипеток, ряд флаконов, шприцы в 1 и 5
см3,
морские свинки весом в 250— 300
г
и сыворотка, силу к-рой, указанную’ на этикетке, надлежит проверить. Доза токсина для опыта (Pd—Prufungsdosis) устанавливается по стандартной сыворотке, которая разводится физиол. раствором так, чтобы в 1
см3
разведения содержалась 1 единица антитоксина (АЕ по Эрлиху). Сначала надлежит определить дозу токсина, к-рая точно нейтрализуется иммунной единицей (АЕ), т. е. от подкожного введения к-рой вместе с АЕ свинка весом в 250—300
г
не только не погибает (L0—Limes Null), но даже на месте подкожного впрыскивания не обнаруживается ни малейшего инфильтрата и вес свинки не падает. Далее устанавливается доза токсина (Lt—Limes mors, смерть), т. е. количество токсина, к-рое в соединении с АЕ содержит как-раз столько-свободного токсина, чтобы убить в течение 4—5 дней свинку весом в 250—300
г.
Эта доза и должна применяться при титровании испытуемой антидифтерийной сыворотки. Последняя разводится так, чтобы в определенном количестве жидкости (для однообразия результатов принято 4
см3)
содержалась 1 антитоксическая единица (АЕ). Напр. если сыворотка содержит в 1
см3
300 АЕ, то она разводится в 300х4=в 1.200 раз. Такое разведение содержит в 4
см3
одну АЕ. Чтобы избежать больших объемов жидкости, употребляется двойное разведение: в 1-й пузырек вливают 99
см3
физиол. раствора и 1
см3
сыворотки; из этого разведения 1
см3
переносится во 2-й флакон с 12
см3
(в нашем случае) физиол. раствора, и получается желаемое разведение сыворотки в 1.200 раз. Если из 2-го разведения взять 4
см3,
то в них будет заключаться 1 АЕ. К этому количеству жидкости с помощью точной пипетки прибавляют дозу токсина, установленную по стандартной сыво -
ротке, и после тщательного смешивания смесь оставляют на 15—30 мин. при комнатной t° и затем вводят под кожу живота морской свинки весом в 250—300
г.
Та сыворотка считается удовлетворительной, смесь к-рой с токсином не убивает свинку; инфильтраты и кахексия не принимаются во внимание. На самом же деле согласно ранее сказанному уже та сыворотка заключает предположенное количество единиц, от смеси к-рой с токсином свинка весом в 250
г
умирает на 4—5-й день. Т. о. при выживании получается нек-рый избыток антитоксина (около 10%), идущий на покрытие убыли антитоксинов при хранении и пересылке. По принятому в СССР положению 1
см3
дифтерийной сыворотки должен содержать не менее 300 антитоксических единиц. Сыворотки должны присылаться на контроль не ранее как через 4 месяца с момента их приготовления, когда они делаются устойчивыми по своей силе. Проверка силы дифтерийных сывороток может производиться также по методу Ремера (Ромег): морской свинке вводится внутрикожно 0,1
см3
смеси дифтерийной сыворотки, разведенной в зависимости от указанной силы, и контрольного токсина. Смесь после стояния в течение 15—20 минут впрыскивается ин-тракутанно. Появление в течение 4—-5 дней на месте инъекции инфильтрата или некроза говорит за то, что испытуемая сыворотка слабее указанной силы; в противном случае место укола абсолютно гладко. По способу Ремера на свинке весом в 350—400 г можно произвести контроль 4 различных серий дифтерийной сыворотки, что является большим удобством при ограниченном количестве животных.—Новейший способ определения силы противодифтерийной сыворотки—реакция ф л о к у л я ц и и по Ра-мону (Ramon). По этому способу в серию пробирок наливают по 20
см3
контрольного токсина, добавляют в убывающих количествах (1,5—0,4) испытуемую сыворотку и встряхивают. После нескольких часов пребывания при комнатной t° можно отметить образование хлопьев. Прежде всего хлопья выпадают в той пробирке, где смесь токсина и антитоксина точно нейтрализована. По этой пробирке и производится определение силы сыворотки. Кроме того титрование противодифтерийной сыворотки производится по т. н. методу «кольцепреципитации» (Ген, Цып и Чертков), основанному также на принципе флокуляции. Стандартизация противостолбнячной сыворотки. В СССР определение силы противостолбнячной сыворотки производится по американскому методу Розенау и Андерсона (Rose-nau, Anderson). Принцип этого метода совершенно такой же, как и для титрования противодифтерийной сыворотки. За единицу (АЕ) антитоксина принята 10-кратная доза того минимального количества сыворотки, к-рое предохраняет морскую свинку весом в 350
г
в течение 4 дней от test-дозы столбнячного стандартного токсина (сухой столбнячный токсин, отличающийся большой стойкостью). Test-доза токсина содержит несколько менее 100 минимальных смер – тельных доз. Смесь из 1/10 антитоксической единицы со 100 смертельными дозами содержит свободного токсина как-раз столько, чтобы убить морскую свинку на 4-й день (Lt). Сила испытуемой сыворотки измеряется по токсину, причем пользуются Lt его. Испытуемая сыворотка разводится так, чтобы 1
см3
ее содержал
1/10
АЕ; напр. если сыворотка содержит 150 единиц антитоксина, то ее надо развести в 1.500 раз. 1
см3
этого разведения смешивается с 1
см3
токсина, разведенного таким образом, чтобы он содержал в себе Lt, доливается до 4
см3
физиол. раствором и после часового стояния при комнатной t° вводится морской свинке под кожу живота. В течение 4 дней свинка должна остаться в живых.-—Титрование по немецкому способу основано на принципе нейтрализации Vtoo АЕ возрастающих доз токсина. Испытание производится на мышах. Для контроля приготовляют 2 серии по 8 смесей. В пробирках первой серии содержится 1
см3
разведенной стандартной сыворотки (1 слг8=0,01 антитоксической единицы), во второй серии— разведения испытуемой сыворотки, сделанные согласно указанному на ярлычке числу АЕ в 1
см3
сыворотки. В каждую пробирку обеих серий прибавляют контрольный токсин в возрастающих дозах от 0,08 до 0,15, доливают физиол. раствором до 4
см3
и 0,4
см3
этой смеси вводят двум сериям мышей (весом по 15
г
каждая, всего 16 мышей) под кожу бедра, т. ч. каждая мышь получает 1/1000 АЕ и возрастающие дозы токсина. Наблюдение ведется в течение 5 суток. Если контролируемая сыворотка имеет указанную на ярлычке силу, то все явления у животных идут параллельно в обеих сериях; в противном случае по несовпадению результатов (быстрая гибель мышей) со стандартной сывороткой вычисляется, насколько испытуемая сывор
отка оказалась слабее. Столбнячная сыворотка, так же как и дифтерийная, присылается на контроль лишь через 4 месяца после изготовления. Соотношение между американской и немецкой единицей приблизительно следующее. Если принять величину немецкой единицы за 1, то американская единица будет соответствовать 60—66 единицам. Сила столбнячной сыворотки, изготовляемой в СССР, колеблется между 100 и 600 единиц в 1
см3.
—С тандартизация противодизентерийной сыворотки. В 1926 г. гиг. секцией Лиги наций принят международный метод стандартизации сыворотки. По постановлению этой секции Копенгагенский сан.-гиг. ин-т регулярно рассылает во все центральные ин-ты стандартную антитоксическую сыворотку, содержащую 200 антитоксических единиц в 1
см3.
Сухой дизентерийный токсин, представляющий собой высушенные микробные тела, вытитровывается со стандартной сывороткой. Максимальное количество токсина, в соединении с антитоксической единицей нейтрализующееся настолько, что большинство из 6 мышей остается в живых к 8-му дню, является дозой токсина, употребляемой для испытания сыворотки. Эта доза в смеси с убывающими дозами испытуемой сыворотки, оставляется на
*lt
часа в термостате при 37° и затем в объеме 0,5
см3
вводится в вену хвоста белой мыши весом 14^-18
г.
Минимальное количество сыворотки, предохраняющее мышей от смерти в течение 7 дней, содержит в себе одну единицу антитоксина. В обращение выпускаются сыворотки, содержащие не менее 300 АЕ в 1
см3.
Контроль пр от ив о скарлатинозной сыворотки. Современные противоскарлатинозные сыворотки обычно являются антитоксическими, хотя иногда приготовляются и сыворотки смешанного типа. Общепринятого метода контроля пока еще нет. Применяются следующие способы: 1.& Метод «у г а ш е н и я сыпи» Шульце-Чарлтона (Schultze-Charlton). В разгар высыпания скарлатинозному больному вводится в толщу кожи испытуемая леч. сыворотка в различных разведениях в объеме 0,1
см3.
Предельное разведение сыворотки, вызывающее феномен «угашения» сыпи (по-бледнение кожи на соответственном участке), является титром данной сыворотки.— 2.& Американский метод на козах, предложенный Уодсуортом, Кирк-брайдом и Уеллером(\7ас18\УогШ, Kirkbride, Weller) и разработанный С. В. Коршуном и В. А. Крестовниковой. Кожа особой породы коз (в СССР наиболее подходящими оказались зааненская и ярославская породы) является чувствительным органом по отношению к «скарлатинозному» токсину (токсину, получаемому при выращивании в определенных условиях гемолитического стрептококка, выделенного от скарлатинозных б-ных). При введении в кожу такой чувствительной козы «скарлатинозного» токсина в определенной дозе (3 кожных для человека дозы) на месте укола через сутки появляется покраснение, занимающее площадь в 1, 5—2
см
в диаметре. При смешении антитоксической скарлатинозной сыворотки со «скарлатинозным» токсином последний нейтрализуется, и при введении в кожу козы реакция отсутствует. Минимальное количество сыворотки, нейтрализующее 100 кожных для козы доз токсина, принято называть антитоксической единицей. Для титрования сыворотки «скарлатинозный» токсин разводится таким образом, чтобы 100 кожных для козы доз содержалось в 0,05
см3;
различные разведения испытуемой сыворотки также в объеме 0,05
см3
смешиваются со 100 кожными для козы дозами и после 3/4-часового пребывания в термостате в объеме 0,1
см3
вводятся в кожу козе. Минимальное количество сыворотки, нейтрализующее 100 кожных для козы доз, является титром данной сыворотки, т. е. указывает на количество антитоксических единиц в 1
см3
сыворотки. Леч. сыворотка должна содержать не менее 200 антитоксических единиц в 1
см3.
Метод не получил широкого распространения в виду трудности подыскания чувствительных к «скарлатинозному» токсину коз.—3. Американский метод Дик (Dick). Испытание силы сыворотки производится кожной реакцией на чувствительном к «скарлатинозному» токсину человеке. Ва – шингтонская федеральная лаборатория в наст, время приготовила стандартную сыворотку, содержащую 40 антитоксических единиц в 1
см3.
Антитоксическая скарлатинозная единица по этому методу нейтрали^ зует 50 кожных доз. Обычно американская сыворотка приготовляется в 10—15 раз крепче. — 4. Метод флокуляции in vitro дал хорошие результаты в руках нек-рых авторов (Рамон, Халяпина), но недостаточно разработан. Также недостаточно разработанным является англ. метод (О ‘Brienn, Okell, Parisch) на кроликах. Обилие применяемых методов говорит о том, что все они далеки еще от с